文摘
目的
我们的目标是修改急性呼吸窘迫综合征(ARDS)的定义使用概念模型将信度和效度,和一个新的迭代方法的正式评估的定义。
方法
重症监护医学的欧洲社会识别三把椅子广泛的专业技术在ARDS选择创建的参与者和议事日程。经过2天的共识讨论草案的定义是,然后接受经验评估共识修订紧随其后。
结果
ARDS的柏林定义维护链接之前定义的诊断标准时间、胸部成像、水肿、起源和血氧不足。可能ARDS患者如果发病一周内已知的临床侮辱或新/呼吸道症状恶化。双边的混浊在胸部标准,参考的胸片了加强inter-observer可靠性。肺动脉楔压标准液压水肿了,说明短文创建指导判断呼吸衰竭的主要原因。ARDS是明显的,如果没有风险因素,客观评价(例如,超声心动图)需要帮助排除液压水肿。最低级别的呼气末正压通气和互斥PaO2/ FiO2阈值选择不同级别的ARDS严重性(轻度、中度、重度)更好的分类不同的结果和潜在的患者对治疗的反应。
结论
这个小组解决的一些局限性合并ARDS之前定义的当前数据,生理概念,柏林和临床试验的结果发展定义,这将促进情况下识别和更好的治疗方案匹配程度试验和临床实践的研究。
介绍
第一个定义的急性呼吸窘迫综合征(ARDS)日期在1967年阿什宝和他的同事描述严重急性呼吸衰竭患者12时(1]。这些患者有严重低氧血症耐火材料补充氧气,但在某些情况下是响应的应用呼气末正压通气(偷看)。广泛的肺部炎症、水肿和透明膜解剖观察。
提出了未来25年的一些定义,但没有单一的定义ARDS广泛接受和使用。1994年,广泛共识取得欧美共识会议(AECC)发表了一个定义2,3]。这一组定义ARDS的急性发作血氧不足(动脉氧的分压比的启发(PaO氧气2/ FiO2]≤200毫米汞柱),双边浸润额胸部x光片,如果没有高血压左心室。他们还定义了一个新的交叉实体称为急性肺损伤(ALI),使用相同的变量,但与低氧血症(PaO不那么严格的标准2/ FiO2≤300毫米汞柱)。
AECC定义已被临床医生和研究人员广泛采用和促进了ARDS的收购大量的数据在接下来的二十年。然而,在此同时,许多问题AECC定义变得明显(4,5]。评估的定义作为一个整体,一个修改AECC定义(使用整个应用回顾性ICU停留时间和要求的四方形领空疾病)与参考标准的弥漫性肺泡损伤出现在尸体解剖。在这些条件下AECC定义表现相当好,敏感性为75%,特异性为84% (6]。然而,当AECC定义标准严格应用(双边胸部x光片浸润)每天,灵敏度保持合理的为84%,但只有51%的特异性明显降低(7]。此外,阿里,使用AECC定义标准,病因是由临床医生,尤其是温和低氧血症患者(即的子群。,PaO2/ FiO2201 - 300年)(7- - - - - -9]。
AECC定义要求呼吸衰竭是急性发作,但没有明确定义的具体时间(例如,几小时,几天,或周)。因为PaO血氧不足标准产生了担忧2/ FiO2可能随FiO2,也为了其他呼吸机设置,尤其是窥(10- - - - - -15]。胸部x光片标准只有温和inter-observer可靠性即使应用专家,尽管这可以通过使用改进的射线照片的训练集16,17]。最后,尽管AECC定义包括肺动脉楔压(PAWP)≤18毫米汞柱(测量),患者标志ARDS的结果往往有高架PAWP因为胸腔压力升高和/或积极液体复苏(18,19]。
由于这些原因,因为所有的定义应该定期检查和调整,以反映新的信息和经验,我们召开了一次共识面板地址前面的AECC定义的局限性并提出修正。柏林的方法论和实证评价定义已经出版之前(22];当前的出版提供了一个扩展的讨论背后的基本原理的发展柏林的定义,并提供进一步的补充材料(例如,典型的例子从ARDS患者胸部x光检查)促进其应用。
方法
如前所述(22],ARDS的面板修改定义用于临床实践和临床研究,使用概念模型结合可靠性、有效性和一种新的迭代方法,包括正式的评估的定义使用大型军团的综合症患者(如最初使用AECC定义定义)。工作组是由重症监护医学的欧洲社会(ESICM),支持过程提供一种无限制的补助金和所有必要的物流。这个格兰特覆盖的成本面对面的会议还在柏林和随后的电话会议。没有收到行业支持的任何部分的过程。
ESICM确定三把椅子ARDS专长,临床流行病学、生理、和临床试验(拉涅利,·鲁本菲尔德和汤普森),他们选择了参与者和创造了议程。小组成员选择(附录中列出)是基于他们公认的专长领域的ARDS,并确保知识的多样性。具体地说,椅子试图达到一个平衡的观点,临床医生、实验、流行病学家、生理学家,和基本的科学家。椅子有兴趣的还包括两个初级成员ARDS。
所有修改ARDS的定义是基于的原则综合症的定义必须满足三个条件:可行性、可靠性和有效性20.]。可行的定义应该依靠诊断测试和/或重症临床经常使用的数据等,可以在短时间内促进临床试验注册。因为它是必不可少的研究人员识别患者在研究类似的特征,并为临床医师应用研究的结果在床边,综合症的定义必须可靠衡量inter-observer协议。最常见的技术建立诊断标准的有效性需要黄金标准,在ARDS是不可用的。然而,许多症状在医学上没有定义一个参考标准包括抑郁,脓毒症和肺炎。各种存在间接评估有效性的方法(如脸、构造、预测和同时效度)的症状没有参考标准(表1)。除了可行性和可靠性,我们强调表面有效性(“概念模型”的临床医生认识到综合征)和预测效度(综合症定义的能力来预测结果和/或对治疗的反应)。最后,专家组认为定义的任何修改应兼容之前的定义来促进老年研究的解释。
每个主持人被要求评估潜在的定义标准使用一个框架关注可靠性、可行性和有效性。我们使用了一个非正式的共识技术涉及整个小组讨论主持的其中一把椅子上,进行面对面和电话会议。共识是证明了一致同意在选项。问题有争议时,个人是的/不投票,确保所有小组成员有机会表达他们的意见。
经过2天的面对面的讨论(2011年10月30日9月1日)在柏林,德国提出了定义(草案21]。这个草案的定义是评估使用现有ARDS病人数据库,以确定特征在每个类别的ARDS死亡率并检查预测效度。最后,小组开会由多个电话会议在2012年2月进行进一步讨论,生成最终的柏林ARDS的定义(22]。之前提交出版的共识定义经历了一个独立的同行审查的过程和随后的认可每个ESICM,美国胸科学会,和危重病医学的社会。
ARDS的概念模型
表面有效性来源于了解临床医生认识到患者的综合征,因此,相当多的讨论集中在发展ARDS的概念模型。专家组一致认为,ARDS是一种急性弥漫性肺损伤与诱发危险因素有关,表现为炎症导致肺血管通透性增加和损失的充气的肺部组织。临床综合征的特点是低氧血症和双边射线混浊(23)(使用标准x射线胸透或计算机断层扫描(CT)扫描),与几个相关生理紊乱,包括:增加肺静脉血掺杂,增加了生理死腔,减少呼吸系统顺应性。急性期的形态特征是肺部水肿、炎症、透明膜、肺泡出血(即。弥漫性肺泡损伤)[24]。
ARDS的常见危险因素有很多,其中AECC定义分为直接和间接肺损伤类别。尽管一些实验和临床研究表明适度的炎症反应和射线照相模式总体差异以及生理反应通气治疗,直接和间接类别重叠很大程度上,委员会决定不包括直接和间接ARDS柏林定义(表中不同的实体2)。识别风险因素导致ARDS的个体病人,无论其直接或间接的性质,而服务指导治疗潜在疾病导致ARDS。
柏林ARDS的定义
由此产生的“柏林定义”发表之前,表中列出3(22]。三个互斥的类别的轻微、中等和严重ARDS创建提供更好的预后和治疗选择的分离。基本原理、争议和建议为每个诊断标准将在以下部分中讨论。
原始AECC定义声明,ARDS的发病是急性,排除慢性肺疾病,可引起血氧过低的呼吸衰竭,但是,它没有一个明确的时间框架。观测数据表明,大多数在72 h ARDS患者识别的识别潜在的风险因素,几乎所有患者确认7天内(25,26]。委员会因此“急性发作”定义为ARDS的发展在1星期内已知的临床侮辱或新/呼吸道症状恶化。
AECC定义需要双边浸润符合肺水肿额胸片,但贫穷inter-observer重症可靠性在使用这个定义解释胸片等和放射科医生16,17]。来帮助解决这个问题小组试图使胸部则更显式指定,它应该包括双边的透明一致不能完全解释积液的肺水肿,肺大叶性/崩溃,或结节/大众在胸部作为ARDS的定义标准,同时也认识到,混浊在CT扫描可以代替如果可用。CT扫描异常并不包括在定义的核心部分定义,因为他们不认为可行的当前时间由于担心安全,成本,和缺乏广泛的可用性。此外,加强inter-observer可靠性,包括一组胸片的面板是说明性的判断图像的频谱是一致的,不一致的或模棱两可的ARDS的诊断(见在线补充图片和评论陪同)。委员会考虑更广泛的透明(即要求。,至少有三个象限)定义严重ARDS;然而,这并没有改善死亡率的预测效度,后被进一步共识讨论(22]。
与AECC定义,专家组认为水压水肿(即。,cardiac failure or fluid overload) is one of the most common alternative diagnoses in patients presenting with ARDS. However, given the declining use of pulmonary artery catheters worldwide and the recognition that hydrostatic edema and ARDS may coexist [18,19),肺动脉楔压(PAWP)则被删除。委员会因此决定患者呼吸衰竭不能完全解释为心脏衰竭或液体超负荷根据治疗医生使用所有可用的数据可能有资格为ARDS。然而,如果没有明显的ARDS的已知病因学的风险因素(表2),客观评价心脏功能(例如,超声心动图或测量心输出量)需要帮助排除液压水肿继发于心力衰竭。为了提高可靠性和清晰这一标准来判断,该小组还开发了一系列临床小插曲说明情况,不符合ARDS基于排除液压水肿(在线补充)。
由PaO AECC定义分类ARDS2/ FiO2比无论偷看的水平(2]。因为偷看可以影响PaO的可靠性和特异性2/ FiO2,对ARDS的严重程度进行分类10,13),最低级别的5厘米H2O窥视(或非侵入性CPAP轻微ARDS)已包括在更新定义。偷看的小组最初提出了一个要求≥10厘米H2O的标准严重ARDS集团,但后来放弃了,因为它没有改善死亡率的预测效度的组内PaO患者2/ FiO2≤10022]。
最近的数据表明,对于一个给定的PaO2/ FiO2比,高FiO2与一个更高的死亡率(15];然而,由于临床医生通常滴定FiO2保持PaO260 - 80毫米汞柱之间,大多数患者PaO2/ FiO2≤100毫米汞柱已经FiO20.7或更高版本。因此,为了避免额外的复杂性,可能减少了可行性;委员会没有添加一个最低FiO2要求定义。
一些医生依靠氧合血红蛋白饱和度通过脉搏血氧仪(热点2)而不是动脉血气分析监测动脉氧合,尤其是在那么严重ARDS患者。的热点;2/ FiO2比与其PaO2/ FiO2比(27),所以可行性的定义可以增强使用热点2代替PaO2。但是,在某些病人热点2不整合与PaO2(28]。特别是,与热点2/ FiO2病人接受FiO21.0和热点2100%的可以分为严重ARDS,不管他们的PaO2,因此热点2/ FiO2比率可以分类的病人。因此,委员会不包括热点2/ FiO2作为一个PaO的替代品2/ FiO2在修改后的定义。
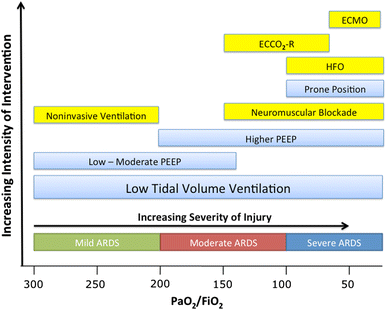
急性肺损伤(ALI)(即。,所有PaO患者2/ FiO2≤300)被撤ARDS的定义,由于知觉,许多临床医生和研究人员认为阿里是一个类别的患者(即。,PaO2/ FiO2201 - 300年),是ARDS分开而不是所有病人的总称(导致频繁使用术语ALI / ARDS AECC没有解释的定义)。这个新的框架下,每个子类ARDS(轻度、中度、重度)被定义为相互排斥的PaO的范围2/ FiO2。轻度ARDS的创建类别正式之前认为的较轻的一种综合症患者但通过应用术语ARDS,它认识到病情的严重程度(死亡率27%22])和反应肺保护性通气(29日]。严重ARDS、两种可能的阈值被认为是PaO2/ FiO2≤150或≤100。小组决定低阈值可以很好地代表了可以考虑哪一个治疗小组,在一些研究中出现严重ARDS是有益的,如容易定位(30.]。委员会认为,新的PaO2/ FiO2阈值选择不同层次的ARDS严重性可能有助于患者分类对不同的治疗方法(无花果。1)。
调整治疗方案与柏林(改编自定义48与许可])。此图描绘了潜在的治疗选项根据ARDS的严重程度。盒子用黄色代表疗法,在专家组的意见仍然需要前瞻性的临床试验中得到了证实。这个图只是一个模型基于当前可用的信息。在未来几年,图的各个方面可能会变化;提出否决可能移动,和一些治疗方法可能不是很有用,而其他可能被添加
额外的生理测量
高原压力(如测量后end-inspiratory停顿)反映了潮汐的体积,偷看,合规的呼吸系统和与死亡率(31日]。理论上,常规测量的高原压力可以帮助分类基于患者ARDS严重性,援助设置通气策略,和疾病随着时间的演变。然而,高原压力不是经常用一些中心,和特定的使用呼吸机模式(例如,压力控制通气)或通风与自主呼吸支持(如压力支持通气)呈现高原压力的测量不切实际。
静态呼吸系统遵从性(即。,the change in lung volume for a given driving pressure defined as tidal volume divided by plateau pressure minus PEEP) reflects the degree of lung volume loss. Although this measurement has the same concerns regarding feasibility as plateau pressure, the panel initially suggested including it (compliance <40 mL/cmH2O)作为严重ARDS的定义的一部分,基于之前定义为ARDS(使用一个评分系统32]。增加死腔是常见的ARDS患者和死亡率增加有关33,34]。测量死腔,然而,是具有挑战性的,感觉不是在日常临床实践中是可行的。作为代理的死腔,一分钟通风帕科纠正2(计算每分通气量×帕科2/阈值40毫米汞柱)> 10 L / min最初选择的面板定义(35),因为它对应大约50%的死亡空间分数,在一项研究与死亡率增加有关(34]。然而,静态合规和纠正每分通气量下降从柏林最终定义,因为它们增加了复杂性并没有提高预测效度。面板是小心翼翼地强调,排除这些变量的定义没有办法减少它们的重要性在日常ARDS患者的评估和管理。
其他标准
我们考虑一些额外的潜在诊断标准包含在柏林的定义;这些的完整列表和排斥的原因如表所示4。没有血管的肺水(EVLW)可以使用transpulmonary测量热稀释法技术和高水平与ARDS患者的死亡率增加相关(36]。目前,技术测量EVLW相对昂贵,入侵,没有广泛使用,具有重要的方法论的限制(37),所以我们不包括它的定义。专家组还考虑潜在的生物标记(例如,il - 6, TNF-α)或遗传标记(例如,ACE基因多态性)帮助ARDS患者的识别。尽管大量的候选生物标志物和遗传标记研究[38,39),目前没有足够的用于ARDS的诊断敏感性和特异性(38- - - - - -40]。
尽管ARDS是弥漫性肺泡损伤的病理关联(爸爸),研究表明只有温和的协议ARDS和爸爸尸检的临床诊断6]。小组的成员并不完全同意爸爸ARDS的唯一病理关联,和一些被认为是肺炎和non-cardiogenic水肿时兼容ARDS临床标准得到满足。因此,自从使用肺活检病理诊断为ARDS可能与并发症的风险增加有关,该委员会不包括在定义。目前,肺活检可能是持久ARDS患者的病因不明,排除了一个潜在的病因,可能应对特定的治疗(41,42]。
连续为ARDS表型定义
先前的调查人员猜测死亡率的差异报告观察性研究和变量在临床试验中对治疗的反应可能是由于血氧不足的任意阈值的定义,以及变化的解释其他诊断标准43]。专家组认为定义一个连续的表现型的可能性(例如,概率和/或严重ARDS定义数字分数),而使用一个简单的是或否的定义,这可能更好的代表ARDS的临床表现(44]。鉴于该需要复杂性的增加,随着不确定性的意义和重要性中间表型(如会议氧化标准但模棱两可的胸部x光发现),该委员会认为进一步的研究是需要再考虑一个连续的表型在ARDS的定义。
柏林的定义和未来ARDS的临床试验
专家组建议未来试验被设计使用一个或多个人口ARDS子组为基础的研究,这可能是用生理和/或其他标准进一步细化具体的假定的作用机理研究干预(例如,il - 6水平il - 6的审判拮抗剂;更严格的研究体外膜肺氧合血氧不足标准)(图1)。ARDS的不同类别(轻度、中度、重度)对分层在临床试验中也可能有用。
未来的研究在柏林ARDS的定义
一些重要的第一步已经在确定病人的频率分布在每个子群ARDS使用这个新定义的22]。此外,这项工作为研究者提供一个想法的每个风险类别的患者比例可能有资格得到包含在未来的治疗干预的临床试验和观察性研究。
柏林定义的实现将随着时间的推移,允许正式评估的可行性(包括障碍/主持人去吸收的临床实践和研究设置)和可靠性的情况下识别基于每个主要的诊断标准(例如,胸部x线摄影混浊,排除液压肺水肿)。柏林的脸和内容效度的定义可以通过反馈评估从一个更广泛的临床医生和研究人员小组。最后,定义可能的效标效度评估相比,解剖发现,从已有的数据和在将来的研究中。
正在进行的研究的识别准确诊断或预后基因多态性或生物标记ARDS可能有助于进一步改善在未来定义的特异性。同样的,可再生的和有效的方法直接测量的肺血管通透性或肺血管外的水将在当前重要进展的评估方法的存在和起源肺部水肿,并可能被纳入未来ARDS的定义。
结论
柏林定义了实现更可靠的定义,以促进情况下识别和更好的治疗方法和临床结果的严重性疾病类别。重要的增量的进步这ARDS的定义包括:注重可行性、可靠性、和有效性在定义发展;经验评估过程的整合在精炼的定义(22];和创建显式的例子来帮助应用影像学和水肿起源标准(在线补充)。柏林定义需要发展新的信息和经验是获得广泛实现在临床实践和研究,以及开发新的诊断工具(如成像技术,生物标志物,肺血管外的水测量)这可能被视为包含在未来ARDS的定义。
缩写
- ARDS:
-
急性呼吸窘迫综合征
- “欧洲:
-
体外生命支持
- FiO2:
-
氧气的启发
- 高频振荡器:
-
高频振荡
- PaO2:
-
动脉氧气分压
- 窥:
-
呼气末正压通气
引用
阿什宝DG,毕格罗DB,琐碎的TL,莱文在成年人(1967)急性呼吸窘迫。柳叶刀2:319 - 323
伯纳德•GR阿提加斯,布里格姆KL,三面锉J, Falke K,哈德逊L,拉米M, LeGall JR,莫里斯,Spragg R (1994) ARDS欧美共识会议。定义、机制相关的结果,和临床试验的协调。地中海是J和保健149:818 - 824吗
阿提加斯,伯纳德•GR三面锉J,更有D, Gattinoni L,哈德逊L,拉米M,马里尼JJ, Matthay妈,平斯基先生,Spragg R,苏特(1998)下午欧美共识会议ARDS,第2部分:通气,药理学,支持性疗法,研究设计策略,恢复和重建的相关问题。急性呼吸窘迫综合征。地中海是J和保健157:1332 - 1347吗
小Phua J,十二月,Adhikari NK,弗里德里希·乔,福勒RA,辛格JM,尺度,Stather博士,李,琼斯,Gattas DJ,哈雷特D,汤姆林森G,斯图尔特TE,弗格森ND(2009)急性呼吸窘迫综合征死亡率降低了时间吗?:系统回顾。地中海是J和保健179:220 - 227吗
利维毫米(2004)偷看ARDS-how多少才够呢?郑传经地中海J 351:389 - 391
埃斯特万,Fernandez-Segoviano P, Frutos-Vivar F, Aramburu是的,纳胡拉L,弗格森ND,阿里我中意F,里奥斯,F(2004)比较急性呼吸窘迫综合征的临床标准与解剖结果。安实习生地中海141:440 - 445
弗格森ND, Frutos-Vivar F, Esteban Fernandez-Segoviano P, Aramburu是的,纳胡拉L,斯图尔特TE(2005)急性呼吸窘迫综合征:根据临床医生识别和诊断的准确性三个临床定义。暴击治疗地中海33:2228 - 2234
克里斯蒂米凯尔森Kalhan R, M, Dedhiya P J, Gaughan C, Lanken PN,芬克尔B,疾驰R, Fuchs BD(2006)未充分利用的肺保护性通气:分析潜在的因素来解释医生的行为。暴击治疗地中海34:300 - 306
卡特·鲁本菲尔德GD,库珀C, G,汤普森BT,哈德逊LD(2004)障碍为急性肺损伤患者提供lung-protective通风。暴击治疗地中海32:1289 - 1293
维拉J, Perez-Mendez L, Kacmarek RM(1999)目前的定义急性肺损伤和急性呼吸窘迫综合征并不反映他们真实的严重程度和结果。重症监护医学25:930 - 935
高达,女士Klocke RA(1997)指数的变化在成人呼吸窘迫综合征血氧不足。暴击治疗地中海25:41-45
弗格森ND, Kacmarek RM, Chiche j d,辛格JM,哈雷特特区Mehta年代,斯图尔特TE(2004)筛选ARDS患者使用呼吸机设置标准化:对注册临床试验的影响。重症监护医学30:1111 - 1116188金宝慱官网下载
维拉J, Perez-Mendez L,洛佩兹J,贝尔达J,布兰科J, Saralegui我Suarez-Sipmann F,洛佩兹J, Lubillo年代,Kacmarek RM(2007)早期偷看/供给试验确定不同程度的急性呼吸窘迫综合征患者的肺损伤。地中海是J和保健176:795 - 804吗
Aboab J, Louis B, B琼森,Brochard L (2006) PaO 2 /供给之间的关系比和供给:一个数学描述。重症监护医学32:1494 - 1497
布里托,斯穆特E,刘KD,汤普森BT, Checkley W,布劳尔RG,美国国立卫生研究院的急性呼吸窘迫综合征网络调查(2011)呼气末正压通气和Fio的价值2在急性呼吸窘迫综合征的定义标准。暴击治疗地中海39:2025 - 2030
考德威尔·鲁本菲尔德GD, E, Granton JT,哈德逊LD, Matthay马(1999)Interobserver可变性在应用影像学对ARDS的定义。胸部116:1347 - 1353
米德,库克RJ Guyatt GH,格罗尔RJ, Kachura JR Bedard说,库克DJ, Slutsky,斯图尔特TE (2000) Interobserver解释胸片变化为急性呼吸窘迫综合征的诊断。地中海是J和保健161:85 - 90吗
弗格森ND,米德,哈雷特,斯图尔特TE(2002)高值的肺动脉楔压患者急性肺损伤和急性呼吸窘迫综合征。重症监护医学28:1073 - 1077
国家心肺和血液研究所急性呼吸窘迫综合征ARDS临床试验网络,惠勒美联社,汤普森BT,伯纳德•GR Schoenfeld D,魏德曼惠普,deBoisblanc B,康纳斯房颤,海特RD,哈拉宾(2006)肺动脉和中央静脉导管引导治疗急性肺损伤。郑传经地中海J 354:2213 - 2224
Rubenfeld GD(2003)急性肺损伤的流行病学。暴击治疗地中海31(增刊):S276-S284
ESCIM国会突出部分(2011)ARDS:“柏林”定义。可以在:http://www.esicm.org/07-congresses/0A-annual-congress/webTv.asp。2015年6月4日通过
ARDS定义特遣部队(2012)急性呼吸窘迫综合征:柏林的定义。JAMA 307:2526 - 2533
mcmahon Hansell DM, Bankier AA, H, McLoud TC,穆勒问,雷米J (2008) Fleischner社会:胸成像的术语表。放射学246:697 - 722
Katzenstein AL,布卢尔厘米,Leibow AA(1976)弥漫性肺泡氧气破坏而言作用,冲击和相关因素。复习一下。是中草药85:209 - 228吗
哈德逊LD、Milberg JA事务所Anardi D,徘徊RJ(1995)急性呼吸窘迫综合征的临床发展的风险。地中海是J和保健151:293 - 301吗
Gajic O,达巴格啊,公园PK, Adesanya, Chang SY,侯P,安德森H 3日,霍斯JJ,米凯尔森我,非犹太人NT,龚MN, Talmor D, Bajwa E,沃特金斯TR, Festic E, Yilmaz M, Iscimen R,考夫曼哒,埃斯珀,Sadikot R,道格拉斯·我Sevransky J, Malinchoc M,美国关键的疾病和损伤试验分组:肺损伤预防研究调查人员(USCIITG-LIPS)(2011)的早期识别患者急性肺损伤的风险:评估肺损伤预测分数多中心队列研究。地中海是J和保健183:462 - 470吗
大米TW,惠勒美联社,伯纳德GR,海登DL, Schoenfeld哒,器皿磅,美国国立卫生研究院,国家心脏,肺和血液研究所ARDS网络(2007)比较热点的2/ FIO2比和PaO2 /供给比急性肺损伤患者或ARDS。胸部132:410 - 417
塞尔夫德Louw范,Cracco C, C, A, Harf Duvaldestin P,勒麦尔F, Brochard L(2001)在重症监护室脉搏血氧测量的准确性。重症监护医学27:1606 - 1613
急性呼吸窘迫综合征网络(2000)较低的通风潮汐卷较之传统潮汐卷对急性肺损伤和急性呼吸窘迫综合征。郑传经地中海J 342:1301 - 1308
Sud年代,弗里德里希·乔,Taccone P et al(2010)倾向通风可以减少急性呼吸衰竭患者的死亡率和严重的低氧血症:系统回顾和荟萃分析。重症监护医学36:585 - 599
海格DN,克里希杰,海登DL,布劳尔RG(2005)潮气量减少急性肺损伤患者当高原压力不高。地中海是J和保健172:1241 - 1245吗
穆雷摩根富林明,Matthay妈,卢斯JM,电影先生(1988)扩大成人呼吸窘迫综合症的定义。我和牧师说138:720 - 723吗
Gattinoni L, Vagginelli F, Carlesso E, Taccone P,孔蒂V, Chiumello D, F Valenza, Caironi P, Pesenti, Prone-Supine研究小组(2003)降低帕科2卧姿是预测急性呼吸窘迫综合征的改善结果。暴击治疗地中海31:2727 - 2733
Nuckton TJ,阿隆索JA Kallet RH,丹尼尔•BM Pittet肯尼迪,艾斯纳博士Matthay马(2002)肺静区分数作为死亡的危险因素在急性呼吸窘迫综合征。郑传经地中海J 346:1281 - 1286
Wexler人力资源,洛克(1981页)一个简单的公式调整动脉二氧化碳张力。可以Anaesth Soc J 28:370 - 372吗
普费弗UJ Sakka SG,鲁尔CC,比尔R, McLuckie,莱因哈特K, Meier-Hellmann(2000)评估心脏前负荷,肺血管外的水单transpulmonary热稀释法。重症监护医学26:180 - 187
De Neef Camporota L, M,比尔R(2012)肺血管外的水在急性呼吸窘迫综合征:潜在的临床价值,假设和局限性。暴击治疗16:114
Barnett N,器皿磅(2011)生物标志物在急性肺injury-marking向前进步。暴击保健诊所27:661 - 683
弗洛雷斯C, Pino-Yanes MM, Casula M,维拉J(2010)急性肺损伤的基因:过去、现在和未来。密涅瓦Anestesiol 76:860 - 864
Calfee CS,器皿磅,Glidden DV,艾斯纳医学博士,帕森斯PE、汤普森BT, Matthay马(2011)使用的风险重新分类与多个生物标志物改善死亡率预测急性肺损伤。暴击治疗地中海39:711 - 717
Papazian L, Doddoli C、B Chetaille Gernez YL,蒂里翁X,罗氏制药,Donati Y, Bonnety M, Zandotti C,托马斯P(2007)出资开放肺活检的结果提高了急性呼吸窘迫综合征患者的生存。暴击治疗地中海35:755 - 762
Papazian L,托马斯P, Bregeon F, Garbe L, Zandotti C,勒索克斯P, Gaillat F, Drancourt M, Auffray JP, Gouin F(1998)开放肺活检在急性呼吸窘迫综合征患者。麻醉学88:935 - 944
克劳斯PA, Lipman J,李CC,威尔逊,Scribante J,巴尔J, Mathivha LR,布朗JM在Baragwanath ICU(1993)急性肺损伤。八个月的审计,并呼吁其他器官衰竭的共识成人呼吸窘迫综合症。胸部103:1832 - 1836
沙简历,Lanken PN Localio AR疾驰R,贝拉米年代,科幻,弗洛雷斯C,卡恩JM,芬克尔B, Fuchs BD,加西亚詹,克里斯蒂JD(2010)急性肺损伤分类的另一种方法用于观察性研究。胸部138:1054 - 1061
佩洛西Gattinoni L, Caironi P, P,古德曼LR(2001),计算机断层扫描教导了我们对急性呼吸窘迫综合征?地中海是J和保健164:1701 - 1711吗
考德威尔·鲁本菲尔德GD, E,皮博迪E,韦弗J,马丁DP,内夫M,斯特恩EJ,哈德逊LD(2005)发病率和急性肺损伤的结果。郑传经地中海J 353:1685 - 1693
赵Z, Steinmann D,雷利查斯,古德曼爵士J, K穆勒(2010)偷看滴定法指导下通风均匀性:可行性研究使用电阻抗断层。暴击治疗14:R8
森林AB,弗格森ND(2012)高频通风。:托宾乔丹(ed)机械通气(3理查德·道金斯版)。麦格劳-希尔,纽约媒体
确认
我们感谢塞尔瓦托马焦雷医学博士(麻醉和重症监护,AgostinoGemelli大学医院,UniversitaCattolica▽SacroCuore,罗马,意大利)和安德斯·拉尔森,医学博士,博士(外科学系,麻醉学和危重病医学,乌普萨拉大学,乌普萨拉,瑞典),出席圆桌重症监护医学的欧洲社会的代表。他们没有得到赔偿的角色。我们要感谢凯伦·皮科特MB BCh(医院重症监护、Erasme UniversiteLibre de布鲁塞尔,布鲁塞尔,比利时),她的技术援助,帮助起草一个早期版本的手稿。她收到补偿作用。
的利益冲突
所有作者已经完成并提交有关其潜在的利益冲突披露形式。召开这个会议的目的是欧洲社会和支持财务的重症监护医学(ESICM)。弗格森博士是由加拿大卫生研究院研究新研究员奖(加拿大渥太华)。球迷支持加拿大卫生研究院博士研究奖学金奖(加拿大渥太华)。·鲁本菲尔德博士是由美国国立卫生研究院拨款R01HL067939(美国贝塞斯达)。没有资金组织或者赞助商有任何作用研究的设计和实施;收集、管理、分析、解释数据;或准备,审查或批准的手稿。
作者信息
作者和联系
相应的作者
额外的信息
一项欧洲社会的重症监护医学支持由美国胸科学会、危重病医学的社会和欧洲呼吸协会。
g·d·鲁本菲尔德,b·t·汤普森和v . m .拉涅利的贡献同样这项工作作为工作组的联合主席。
电子辅料
下面是链接到电子辅料。
附录
附录
ARDS工作组成员
椅子
诉马可·拉涅利博士PhD-Department麻醉和重症监护医学,都灵大学意大利都灵
戈登·d·鲁本菲尔德博士MSc-Interdepartmental危重病医学,多伦多大学,多伦多,加拿大
b·泰勒·汤普森MD-Pulmonary /急救护理单元,医学系,马萨诸塞州总医院和哈佛医学院波士顿,MA
参与者
安东内利,MD-Dipartimento di Anestesia e Rianimazione,意大利Cattolica del Sacro库雷,罗马,意大利
安东尼奥·r·Anzueto MD-Pulmonary /急救护理,在圣安东尼奥德克萨斯大学健康科学中心,和南德克萨斯州退伍军人卫生保健系统,圣安东尼奥,德克萨斯州
理查德•比尔MBBS-Division哮喘,过敏和肺生物学,伦敦国王学院和成人重症监护、人的圣托马斯NHS信托基金会,国王卫生伙伴London-UK。
Laurent Brochard博士PhD-Medical-Surgical重症监护室,Hopitaux日内瓦大学医疗瑞士日内瓦
罗伊·g·布劳尔MD-Division肺和危重病医学,马里兰州巴尔的摩约翰霍普金斯大学
路易吉Camporota,医学博士,MRCP-Division哮喘、过敏和肺生物学,伦敦国王学院和成人重症监护、人的圣托马斯NHS信托基金会、国王的健康伙伴London-UK。
安德烈斯埃斯特万博士PhD-Servicio de小心Intensivos、医院大学德赫塔菲。cib de心血管Respiratorias,祝您健康研究所卡洛斯三世,马德里,西班牙
艾迪风扇,MD-Interdepartmental危重病医学、分工和医学系的大学健康网络和西奈山医院,多伦多大学,多伦多,加拿大
尼尔·弗格森博士MSc-Interdepartmental危重病医学、分工和医学系,Respirology分工,大学健康网络和西奈山医院,多伦多大学,多伦多,加拿大
卢西亚诺Gattinoni MD-Istituto di Anestesiologia e Rianimazione,意大利degli某在米兰,米兰,意大利
安德鲁•罗兹MD-Department重症监护医学圣乔治医疗NHS信托,伦敦,英国
阿瑟·s . Slutsky MD-Keenan研究中心的李港发嘉成知识圣迈克尔医院研究所;不同部门间的分工危重病医学,多伦多大学,多伦多,加拿大
jean - louis文森特博士PhD-Department重症监护,Erasme大学医院,大学自由de布鲁塞尔,比利时布鲁塞尔
权利和权限
关于这篇文章
引用这篇文章
菲尔特弗格森风扇,E。,Camporota, L.et al。柏林ARDS的定义:一个扩展原理,理由,和补充材料。重症监护医学38,1573 - 1582 (2012)。https://doi.org/10.1007/s00134 - 012 - 2682 - 1
收到了:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1007/s00134 - 012 - 2682 - 1
关键字
- 诊断
- 国际合作
- 预后
- 呼吸,人工
- 呼吸窘迫综合征,成人
- 风险因素